
Suplementos com cúrcuma podem trazer risco de danos ao fígado, alerta Anvisa
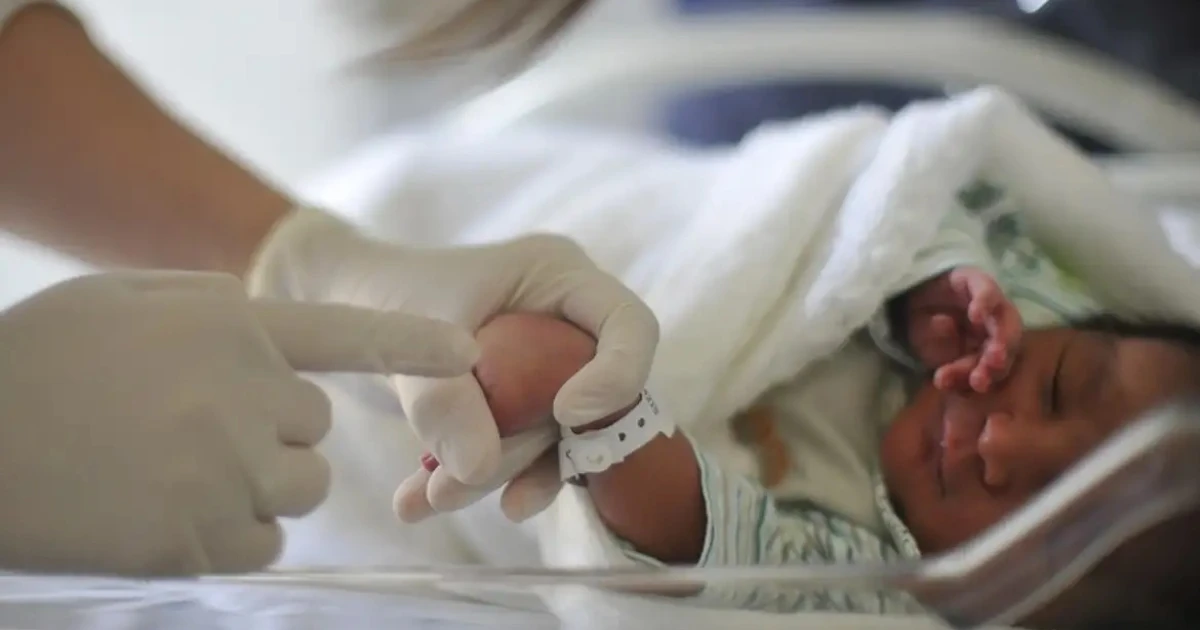
A Agência Nacional de Vigilância Sanitária (Anvisa) emitiu, nesta sexta-feira (6), um alerta de farmacovigilância direcionado a consumidores de medicamentos e suplementos à base de cúrcuma, popularmente conhecida como açafrão. A medida fundamenta-se em investigações internacionais que detectaram casos raros, porém graves, de inflamação e danos hepáticos vinculados à ingestão da substância em formatos de cápsulas ou extratos concentrados.
Entre os principais sinais de toxicidade elencados pelo órgão regulador estão a icterícia, caracterizada pelo amarelamento de pele e olhos, urina escura, náuseas, vômitos, fadiga intensa, perda de apetite e dores abdominais.
A agência esclarece que o risco não se estende ao uso tradicional da cúrcuma como tempero culinário. Segundo a Anvisa, o pó utilizado na preparação de alimentos permanece seguro e não faz parte do alerta, visto que não existem evidências de risco no consumo da planta como alimento ou aditivo alimentar.
A distinção reside no fato de que medicamentos e suplementos apresentam concentrações significativamente mais elevadas do ativo e uma maior capacidade de absorção pelo organismo.
O cenário brasileiro reflete uma movimentação global, uma vez que autoridades sanitárias da Itália, Austrália, Canadá e França também emitiram comunicados após identificarem casos suspeitos de intoxicação do fígado.
a França, a agência ANSES relatou dezenas de episódios de efeitos adversos, incluindo quadros de hepatite, o que levou alguns países a proibirem produtos específicos ou a exigirem alertas de segurança nos rótulos.
No âmbito nacional, a Anvisa já determinou a atualização das bulas dos medicamentos Motore e Cumiah para a inclusão de advertências. Procuradas pela reportagem, a Aché, responsável pelo Motore, e a Legrand Pharma, que fabrica o Cumiah, não enviaram posicionamento até o momento da publicação, permanecendo o espaço aberto para manifestações.
Quanto aos suplementos alimentares, o órgão informou que iniciará um processo de reavaliação e passará a exigir avisos sobre possíveis efeitos colaterais nas embalagens.
A orientação oficial para quem apresentar sintomas é interromper o uso imediatamente e buscar assistência médica. Eventuais suspeitas de reações adversas devem ser registradas nos sistemas VigiMed, para medicamentos, ou e-Notivisa, para suplementos.
Até o fechamento deste alerta, a Anvisa contabilizava 13 notificações no VigiMed relacionadas a medicamentos com cúrcuma e um registro de 2023 no e-Notivisa referente a suplementos, embora nenhum desses relatos específicos no Brasil tenha mencionado hepatotoxicidade até agora.
Com informações de CNN Brasil